Η βαριά μυασθένεια (myasthenia gravis) είναι νόσος της νευρομυϊκής σύναψης (NMJ). Πριν από την περιγραφή της νόσου, είναι σκόπιμη μια ανασκόπηση της φυσιολογικής νευρομυϊκής μετάδοσης των νευρικών ώσεων.
Η άφιξη του δυναμικού ενέργειας στη σύναψη προκαλεί το άνοιγμα τασεοεξαρτώμενων διαύλων ασβεστίου. Το ασβέστιο εισρέει στη νευρική απόληξη και αλληλεπιδρά με πρωτεΐνες SNARE (συναψίνη, συναπτοφυσίνη κ.α.) και τοιουτοτρόπως επιτρέπεται η σύντηξη των συναπτικών κυστιδίων με τη προσυναπτική μεμβράνη με συνέπεια την απελευθέρωση ακετυλοχολίνης (ACh) στη νευρομυϊκή σύναψη (εξωκύτωση Ach).
Η ACh διασχίζει τη συναπτική σχισμή και δεσμεύεται από τους υποδοχείς ακετυλοχολίνης (AChR), οι οποίοι είναι δίαυλοι Na⁺/K⁺ που ενεργοποιούνται από την ACh. Εάν ενεργοποιηθεί επαρκής αριθμός διαύλων (υποδοχείς ακετυλοχολίνης), προκαλείται εκπόλωση της μυϊκής μεμβράνης και διάδοση του δυναμικού ενέργειας κατά μήκος των σωληναρίων Τ της μυϊκής ίνας, με αποτέλεσμα την απελευθέρωση ιόντων Ca²⁺ από το σαρκοπλασματικό δίκτυο και την πρόκληση μυϊκής σύσπασης.
Η ACh στη συναπτική σχισμή υδρολύεται (αδρανοποιείται) από την ακετυλοχολινεστεράση (AChE) και μετατρέπεται σε οξικό και χολίνη. Η χολίνη προσλαμβάνεται από το προσυναπτικό νευρικό άκρο και με το συνένζυμο ακετυλσυνένζυμο Α συνθέτει Ach στο αξονόπλασμα των νευρικών απολήξεων για την επόμενη απελευθέρωσή της στη συναπτική σχισμή.
Η διάσπαση της ACh στη νευρομυϊκή σύναψη είναι απαραίτητη για την αποτροπή παρατεταμένης μυϊκής σύσπασης. Ενδιαφέρον είναι ότι η παρατεταμένη μυϊκή σύσπαση αποτρέπεται, επίσης, από την παρουσία νικοτινικών υποδοχέων ακετυλοχολίνης στην προσυναπτική μεμβράνη, οι οποίοι αναγνωρίζουν την παρουσία ACh στη συναπτική σχισμή και προκαλούν με το μηχανισμό αρνητικής ανάδρασης (Negative Feedback) περαιτέρω μείωση απελευθέρωσης Ach.
Συμπέρασμα
Συμπερασματικά η μυϊκή αδυναμία στη myasthenia gravis οφείλεται στην έλλειψη υποδοχέων ακετυλοχολίνης λόγω καταστροφής τους από αντισώματα. Η ενεργοποίηση των υποδοχέων αυτών, υπό φυσιολογικές συνθήκες, προκαλεί την μυϊκή σύσπαση.
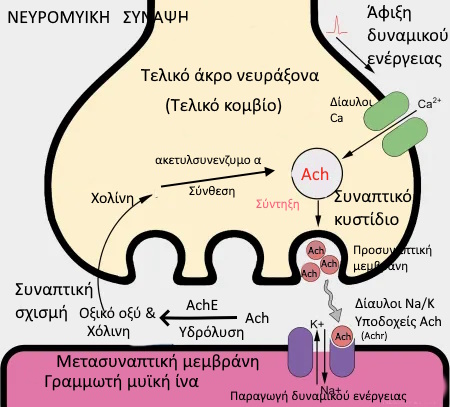
Σχηματική αναπαράσταση της φυσιολογικής νευρομυϊκής μετάδοσης.
Υπάρχουν δύο μορφές βαριάς μυασθένειας: η επίκτητη και η συγγενής.
Η επίκτητη βαριά μυασθένεια είναι ένα αυτοάνοσο νόσημα με κυκλοφορούντα αντισώματα έναντι των νικοτινικών υποδοχέων ακετυλοχολίνης (AChR) στη νευρομυϊκή σύναψη των σκελετικών μυών.
Η συγγενής βαριά μυασθένεια είναι μια κληρονομική διαταραχή που χαρακτηρίζεται από απουσία υποδοχέων ακετυλοχολίνης (AChR) στην μετασυναπτική μεμβράνη.
Έχουν αναγνωριστεί διάφοροι προδιαθεσικοί παράγοντες που μπορεί να οδηγήσουν σε επίκτητη βαριά μυασθένεια. Σε αυτούς περιλαμβάνονται:
- νεοπλασίες (θύμωμα, λειομύωμα, χολαγγειοκυτταρικό καρκίνωμα, αδενοκαρκίνωμα των πρωκτικών σάκων, δερματικό λέμφωμα ή λέμφωμα ΚΝΣ)
- αυτοάνοσα νοσήματα (υποθυρεοειδισμός, υποφλοιοεπινεφριδισμός, αυτοάνοση αιμολυτική αναιμία ή αυτοάνοση θρομβοπενία)
- φάρμακα (π.χ. αμινογλυκοσίδες, αμπικιλλίνη, σιπροφλοξασίνη, ιμιπενέμη). Τα φάρμακα μπορούν δυνητικά να προκαλέσουν ή να επιδεινώσουν τη μυασθένεια gravis.
Υπάρχουν τρεις κλινικές μορφές επίκτητης μυασθένειας gravis: γενικευμένη, εστιακή και κεραυνοβόλος.
Τα ζώα με γενικευμένη μυασθένεια gravis (57%) παρουσιάζουν γενικευμένη αδυναμία και δυσανεξία στην άσκηση, ενώ τα ζώα με εστιακή μυασθένεια gravis (43%) εμφανίζουν εστιακά συμπτώματα λόγω μεγαοισοφάγου (π.χ. αναγωγή, πνευμονία από εισρόφηση) ή φαρυγγικής αδυναμίας (π.χ. σιελόρροια, παλινδρόμηση). Περίπου το 13% των σκύλων με γενικευμένη μυασθένεια δεν παρουσιάζουν φαρυγγική ή οισοφαγική δυσλειτουργία.
Η κεραυνοβόλος μυασθένεια gravis είναι η λιγότερο συχνή μορφή (<5% των περιστατικών) και χαρακτηρίζεται από οξεία και ταχεία εξέλιξη γενικευμένης αδυναμίας, συχνά με τετραπάρεση, αναπνευστική δυσχέρεια και πνευμονία από εισρόφηση. Η μορφή αυτή συνοδεύεται από υψηλό ποσοστό θνησιμότητας.
Στοιχεία του ζώου
Η επίκτητη μυασθένεια gravis μπορεί να εμφανιστεί σε όλες τις ηλικίες αλλά συνήθως εμφανίζεται σε σκύλους συγκεκριμένης ηλικίας (3 ετών ή 10 ετών). Όπως και άλλα αυτοάνοσα νοσήματα, εμφανίζεται συχνότερα σε θηλυκούς σκύλους. Ο υψηλότερος σχετικός κίνδυνος για επίκτητη νόσο παρατηρείται στις φυλές Akita, German Shorthaired Pointer και Chihuahua. Οι German Shepherd και Golden Retriever προσβάλλονται επίσης συχνά. Στις γάτες, οι φυλές Abyssinian και Somali επηρεάζονται συχνότερα.
Η συγγενής μυασθένεια gravis είναι σπάνια και έχει αναφερθεί συχνότερα σε Jack Russell Terrier, Springer Spaniel και Smooth Fox Terrier. Τα κλινικά συμπτώματα παρατηρούνται μόλις το κουτάβι αρχίσει να βαδίζει, σε ηλικία 8–9 εβδομάδων.
Κλινικά συμπτώματα
Τα συχνότερα παράπονα που αναφέρουν οι ιδιοκτήτες είναι η εμφάνιση γενικευμένης αδυναμίας και η απροθυμία για άσκηση (γενικευμένη μορφή βαριάς μυασθένειας) ή αναγωγή και δυσφαγία (εστιακή μορφή). Είναι εξαιρετικά σημαντικό να γίνεται διάκριση μεταξύ εμέτου και αναγωγής.
Τα ζώα με συγγενή μυασθένεια συνήθως προσκομίζονται με γενικευμένη αδυναμία ± αναγωγή στην ηλικία των 8–9 εβδομάδων.
Νευρολογική & κλινική εξέταση
Τα ευρήματα της νευρολογικής εξέτασης συνήθως αντανακλούν μια γενικευμένη νευρομυϊκή διαταραχή. Κατά την ανάλυση της βάδισης παρατηρείται συχνά γενικευμένη αδυναμία ή απροθυμία για άσκηση.
Το ζώο μπορεί μετά την ανάπαυση να έχει φυσιολογική ή δύσκαμπτη βάδιση, η οποία μετά από λίγο χρονικό διάστημα εξελίσσεται σε βηματισμό με μικρά, κοφτά βήματα και τελικά σε αδυναμία βάδισης. Οι αντιδράσεις θέσεις είναι συχνά φυσιολογικές όταν υποστηρίζεται το βάρος του ζώου. Τα νωτιαία αντανακλαστικά είναι φυσιολογικά. Δεν υφίσταται μυϊκή ατροφία.
Μπορεί να παρατηρηθούν δυσφαγία ή δυσφωνία. Η αδυναμία των μυών του προσώπου (εξασθενημένο ή απόν βλεφαρικό αντανακλαστικό) μπορεί να είναι εμφανής, ιδιαίτερα στις γάτες. Στις γάτες παρατηρείται συχνά κάμψη του αυχένα.
Διάγνωση
Βασικός εργαστηριακός έλεγχος
Ο βασικός εργαστηριακός έλεγχος (γενική αίματος, βιοχημικό προφίλ, T4, γενική ούρων) είναι συνήθως φυσιολογικός σε ζώα με βαριά μυασθένεια. Πρέπει να αξιολογείται η παρουσία συνυπάρχουσας νόσου (π.χ. υποθυρεοειδισμός) ή άλλων προδιαθετόντων παραγόντων.
Σε όλα τα ζώα με υποψία βαριάς μυασθένειας πρέπει να γίνονται ακτινογραφίες θώρακος για έλεγχο μεγαοισοφάγου (90% των σκύλων) και δευτερογενούς πνευμονίας από εισρόφηση ή θυμώματος.
Υπερηχογράφημα ή ακτινογραφίες κοιλίας θα πρέπει να πραγματοποιούνται για τον έλεγχο ενδοκοιλιακής νεοπλασίας.
Τίτλος αντισωμάτων έναντι υποδοχέων ακετυλοχολίνης (ARAT)
Ο τίτλος αντισωμάτων έναντι του υποδοχέα ακετυλοχολίνης (ARAT) αποτελεί το «χρυσό κανόνα» για τη διάγνωση της επίκτητης μυασθένειας gravis. Περίπου το 98% των σκύλων με επίκτητη νόσο έχουν κυκλοφορούντα αντισώματα έναντι των AChR. Το υπόλοιπο 2% των ασθενών είτε είναι οροαρνητικοί και πιθανώς έχουν αντισώματα έναντι άλλων μυϊκών πρωτεϊνών είτε η εξέταση πραγματοποιήθηκε πριν αυξηθεί ο τίτλος ARAT.
Όταν το επίπεδο αντισωμάτων έναντι των AChR είναι μεγαλύτερο από 0,6 nmol/L είναι διαγνωστικό για επίκτητη MG στους σκύλους. Για τις γάτες είναι διαγνωστικό όταν είναι μεγαλύτερο από >0,3 nmol/L.
Εάν υπάρχει ισχυρή υποψία επίκτητης MG, ιδιαίτερα όταν ο τίτλος είναι σε μεσαία προς ανώτερα φυσιολογικά επίπεδα, συνιστάται επανάληψη του ARAT σε 3–4 εβδομάδες για αξιολόγηση πιθανής αύξησης.
Υπάρχει φτωχή συσχέτιση μεταξύ του ύψους του τίτλου και της βαρύτητας των κλινικών σημείων. Έχουν παρατηρηθεί ασθενείς με σοβαρή αδυναμία και πνευμονία από εισρόφηση με επίπεδο 1,1 nmol/L που είχαν δυσμενή έκβαση, καθώς και άλλοι με επίπεδο 13 nmol/L με ήπια έως μέτρια αδυναμία που ανταποκρίθηκαν γρήγορα στη θεραπεία.
Ωστόσο, υπάρχει καλή συσχέτιση μεταξύ του τίτλου στον ίδιο ασθενή και της ύφεσης των συμπτωμάτων. Η μείωση του τίτλου υποδηλώνει βελτίωση.
Ο ορός προς εξέταση πρέπει να λαμβάνεται πριν από τη χορήγηση κορτικοστεροειδών.
Τα ζώα με συγγενή MG έχουν αρνητικό τίτλο αντισωμάτων AChR (δεν έχουν υποδοχείς AchR), επομένως η εξέταση αυτή συνήθως δεν πραγματοποιείται, αλλά μπορεί να χρησιμοποιηθεί για τον αποκλεισμό της επίκτητης μορφής σε πολύ νεαρά ζώα.
Δοκιμασία Tensilon
Μπορεί αναμένοντας από το εργαστήριο τον τίτλο αντισωμάτων (AChR) που απαιτεί 5-15 ημέρες, να πραγματοποιηθεί δοκιμασία με χλωριούχο εδροφώνιο (Tensilon test, δεν κυκλοφορεί το φάρμακο πλέον).
Το εδροφώνιο είναι ταχείας δράσης και βραχείας διάρκειας αναστολέας της ακετυλοχολινεστεράσης, η οποία υδρολύει την ακετυλοχολίνη στη συναπτική σχισμή. Η χορήγησή του προκαλεί μείωση της υδρόλυσης της ACh με συνέπεια διατήρηση της Ach στη συναπτική σχισμή και βελτίωση της μυϊκής δύναμης.
Συνιστάται η χορήγηση ατροπίνης (0,02–0,04 mg/kg IM) 15–20 λεπτά πριν τη δοκιμή για την πρόληψη συμπτωμάτων τοξικότητας (σιελόρροια, δακρύρροια, ούρηση, διάρροια, δύσπνοια).
Τεχνική
Ο σκύλος ασκείται μέχρι κόπωσης και στη συνέχεια χορηγείται εδροφώνιο (0,1–0,2 mg/kg IV στους σκύλους ή συνολική δόση 0,25–0,50 mg στις γάτες). Η διαπίστωση μέτριας έως έντονης βελτίωσης της μυϊκής δύναμης είναι ενδεικτική μυασθένειας.
Τα ψευδώς αρνητικά αποτελέσματα είναι συχνά καθώς η δοκιμασία έχει ακρίβεια περίπου 70%. Ψευδώς θετικά αποτελέσματα είναι επίσης δυνατά, καθώς η αυξημένη διαθεσιμότητα ACh μπορεί θεωρητικά να βελτιώσει οποιαδήποτε διαταραχή με αδυναμία, αν και η βελτίωση είναι συνήθως ήπια.
Στο βίντεο παρουσιάζεται μια γάτα με βαριά μυασθένεια και θετική ανταπόκριση στο Tensilon test. (Πηγή. Veterinary neuroanatomy and clinical neurology / Alexander de Lahunta, Eric Glass.3rd ed.)
Δοκιμασία με νεοστιγμίνη
Εάν το εδροφώνιο δεν είναι διαθέσιμο, εναλλακτικά μπορεί να χορηγηθεί νεοστιγμίνη (neostigmine methylsulfate, Prostigmine) σε δόση 20 μg/kg IV. Πρέπει να υπάρχει διαθέσιμος ενδοτραχειακός σωλήνας, λαρυγγοσκόπιο και εξοπλισμός ανάνηψης σε περίπτωση χολινεργικής κρίσης ( η πιθανότητα χολινεργικής κρίσης από τη χορήγηση νεοστιγμίνης είναι μικρή).
Ηλεκτροδιαγνωστικές εξετάσεις
Σε ορισμένες περιπτώσεις απαιτούνται πιο εξειδικευμένες εξετάσεις, οι οποίες προϋποθέτουν παραπομπή σε κτηνίατρο νευρολόγο.
Θεραπεία
Η θεραπεία πρέπει να αρχίζει έγκαιρα και επιθετικά.
Συνιστάται νοσηλεία για τις πρώτες ημέρες για παρακολούθηση λόγω πιθανής επιδείνωσης ή ανεπιθύμητων ενεργειών λόγω των χορηγουμένων φαρμάκων.
Η θεραπεία βασίζεται σε τρεις άξονες:
- Αντιχολινεστερασική αγωγή
- Ανοσοκαταστολή
- Νοσηλευτική και αναπνευστική υποστήριξη
Αντιχολινεστερασική αγωγή
Η πυριδοστιγμίνη (Mestinon) είναι αναστολέας ακετυλοχολινεστεράσης μακράς διάρκειας δράσης και χορηγείται από το στόμα 2–3 φορές ημερησίως (1–3 mg/kg PO BID–TID). Η θεραπεία αρχίζει με χαμηλή δόση η οποία προοδευτικά αυξάνει ανάλογα με την ανταπόκριση.
Σσυμπτώματα χολινεργικής κρίσης λόγω υπερδοσολογίας:
- Σιελόρροια
- Δακρύρροια
- Ούρηση
- Διάρροια
- Δύσπνοια
Το αντίδοτο της χολινεργικής κρίσης είναι η ατροπίνη.
Ανοσοκαταστολή
Η χρήση ανοσοκατασταλτικών φαρμάκων στην επίκτητη MG είναι αμφιλεγόμενη.
Μελέτη σε 53 σκύλους έδειξε αυτόματη ύφεση στο 88% των περιπτώσεων. Πολλοί νευρολόγοι ξεκινούν μόνο με αντιχολινεστερασική αγωγή και προσθέτουν ανοσοκαταστολή εάν δεν υπάρχει ανταπόκριση σε 2–3 ημέρες.
Η πρεδνιζόνη είναι αποτελεσματική αλλά μπορεί:
- Να επιδεινώσει την ήδη υπάρχουσα πνευμονία από εισρόφηση
- Να προκαλέσει νευρομυϊκή αδυναμία αν χορηγηθεί σε υψηλές δόσεις
Άλλα φάρμακα που έχουν χρησιμοποιηθεί:
- Αζαθειοπρίνη
- Μυκοφαινολάτη
- Κυκλοσπορίνη
- Λεφλουνομίδη
Δεν έχει αποδειχθεί υπεροχή κάποιου έναντι άλλου.
Νοσηλευτική & αναπνευστική υποστήριξη
Μπορεί να απαιτηθεί μηχανικός αερισμός σε αναπνευστική αδυναμία.
Συστήνεται σίτιση σε όρθια θέση και παραμονή σε κάθετη στάση για 5–10 λεπτά μετά το γεύμα. Χρήσιμη είναι η καρέκλα Bailey, που διατηρεί τον σκύλο σε κατακόρυφη θέση.
Σε σοβαρές περιπτώσεις μπορεί να χρειαστεί σωλήνας σίτισης ή παρεντερική διατροφή.
Απαραίτητη η καλή φροντίδα κύστης και πρόληψη κατακλίσεων.
Χειρουργική
Η χειρουργική αφαίρεση θυμώματος πρέπει να γίνεται εφόσον είναι εφικτό.
Μελέτες έχουν δείξει ευνοϊκή μακροπρόθεσμη πρόγνωση μετά αφαίρεση θυμώματος, με μέση επιβίωση 635–790 ημέρες στους σκύλους και 1.825 ημέρες στις γάτες.
Μπορεί να υπάρξει πλήρης ύφεση των κλινικών συμπτωμάτων μετεγχειρητικά.
Σημαντικές πληροφορίες
Αν εντοπιστεί εκλυτικός παράγοντας, πρέπει να αντιμετωπιστεί.
Στείρωση θηλυκών σκύλων μόλις σταθεροποιηθεί η MG.
Αποφυγή εμβολιασμών μέχρι να επέλθει ύφεση.
Αποφυγή φαρμάκων που επιδεινώνουν τη MG.
Παρακολούθηση
Η μείωση του τίτλου AChR στον ίδιο ασθενή υποδηλώνει ύφεση.
Η θεραπεία συνεχίζεται μέχρι ο τίτλος να γίνει αρνητικός και επανελέγχεται περιοδικά.
Πρόγνωση
Η πρόγνωση της επίκτητης MG είναι επιφυλακτική λόγω κινδύνου υποτροπιάζουσας πνευμονίας από εισρόφηση.
Εάν δεν υπάρχει μεγαοισοφάγος ή πνευμονία, το ποσοστό αυτόματης ύφεσης είναι υψηλό (~88%) σε 6–8 μήνες.
Η πρόγνωση της συγγενούς MG είναι επιφυλακτική έως φτωχή, αν και ορισμένοι ασθενείς ανταποκρίνονται σε αντιχολινεστερασική αγωγή.
Myasthenia gravis σε γάτες
Οι φυλές Abyssinian και Somali εμφανίζουν αυξημένη συχνότητα. Δεν υπάρχει προδιάθεση φύλου.
Μέση ηλικία έναρξης: 8,6 έτη (εύρος 6 μηνών–15,4 έτη).
Κλινικές μορφές:
Γενικευμένη αδυναμία χωρίς αναγωγή (50%)
Γενικευμένη αδυναμία με αναγωγή (40%)
Εστιακή μορφή με αναγωγή χωρίς γενικευμένη αδυναμία (10%)
Η κάμψη του αυχένα αποτελεί σημαντικό κλινικό σύμπτωμα.
Οι γάτες έχουν μικρότερη συχνότητα μεγαοισοφάγου, καθώς ο οισοφάγος αποτελείται από λείες μυϊκές ίνες.
Οι γάτες έχουν αυξημένη προδιάθεση για θύμωμα. Σε μια μελέτη το 52% των γατιών με MG είχε μάζα στο πρόσθιο μεσοπνευμόνιο Σε όσες έγινε βιοψία, το 97,7% διαγνώστηκε με θύμωμα.
Η μεθιμαζόλη (θεραπεία υπερθυρεοειδισμού) μπορεί να προκαλέσει φαρμακογενή MG.
Η θεραπεία είναι παρόμοια με τους σκύλους (πυριδοστιγμίνη ± ανοσοκαταστολή). Οι γάτες μπορεί να ανταποκρίνονται καλύτερα μόνο σε πρεδνιζολόνη.
Η πρόγνωση στις γάτες είναι πιο επιφυλακτική. Σε μία μελέτηέγινε ευθανασία σε ποσοστό πασχόντων γατιών 52%. Σε αντίθεση με τους σκύλους, υψηλότερος τίτλος AChR συσχετίζεται με χειρότερη επιβίωση.
ΣΗΜΕΙΩΣΗ ΠΡΟΣ ΤΟΥΣ ΑΝΑΓΝΩΣΤΕΣ: Εάν βρείτε λάθος σε αυτό το άρθρο, παρακαλώ στείλε mail (danourdista@gmail.com) για να διορθωθεί. Ευχαριστούμε για την υποστήριξή σας !
